Исследование процессов в трактах теплоэнергетических установок связано с определением различных параметров газового потока, в том числе и состава высокотемпературной газовой смеси. Для контроля токсичности отработавших газов установки также необходимо проводить химический анализ продуктов сгорания. В настоящее время достаточно широкое распространение получили газовые анализаторы, с помощью которых осуществляется химический анализ многокомпонентной смеси. При этом отбор газовой пробы и доставка ее к анализатору осуществляется с помощью специальных охлаждаемых зондов, вводимых в интересующие нас зоны течения. Если отбор пробы производится из высокотемпературной области тракта энергетической установки, то изменение температуры газовой пробы при ее течении в канале зонда сопровождается неравновесным протеканием химической реакции между компонентами пробы. По этой причине химический состав пробы на входе в анализатор будет отличаться от состава газовой пробы в точке ее отбора.
В связи с этим, рассмотрим следующие задачи:
1. Отбор пробы;
2. Нахождение поправочного коэффициента;
3. Анализ пробы.
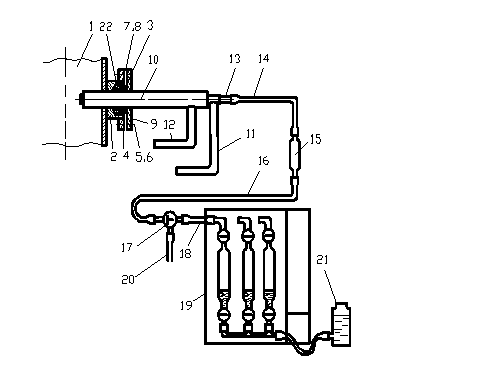
- 1. Отбор пробы осуществляют схемой показанной на рисунке 1.
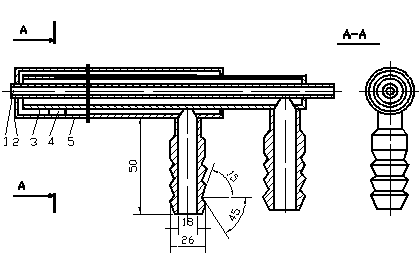
К трубопроводу или к металлическому кожуху канала, по которому движутся анализируемые газы, должно быть приварено уплотняющее устройство (рисунок 2).
При высокотемпературных процессах в газоходе 1 выше 250 0С используют водоохлаждающее газоотборное устройство (рисунок 2), к которому подсоединяют резиновые рукава 11 и 12. подводящий рукав 11 подсоединяют к водопроводу, отводящий рукав 12 – к сливной воронке. Включают охлаждающую воду.
На газоотборную трубку 13 надевают резиновую трубку 14, другой конец которой надевают на заполненный стекловолокном патрон 15. К патрону 15, предназначенному для очистки газов от пыли, присоединяют трубку 16, другой конец которой надевают на отросток трехходового крана 17. На противоположный отросток трехходового крана надевают резиновую трубку 18, а другой ее конец присоединяют к нужной пипетке аспиратора 19. На третий отросток трехходового крана надевают резиновую трубку 20. Свободный конец трубки 20 выводят за пределы помещения, в котором производят отбор проб газа, или относят на расстояние 5 м в направлении ветра, если отбор проб осуществляют на открытом воздухе. Трехходовой кран устанавливают в положение «а».
Рисунок 1. Схема установки для отбора проб газа
Свинтив гайки 6 с болтом 5 уплотняющего устройства 2, снимают нажимной фланец 9, пластину 8 и асбестовую прокладку 7. Вынимают из корпуса уплотнительного устройства нажим 3.
На водоохлаждаемое газоотборное устройство 10 надевают сначала нажимной фланец 9, затем нажимное кольцо 3. Газоотборное устройство вставляют в уплотнительное устройство. На газоотборное устройство наматывают шнуровой асбест с таким расчетом, чтобы после того, как он будет вдвинут в корпус 2, вставленное вслед за ним кольцо 3 выступало из фланца 4 на 5-7 мм. Передвигая кольцо 3 по газоотборному устройству 10,вдвигают кольцо и шнуровой асбест 22 в корпус 2. Прижимают болтами фланец 9. Гайки 6 болтов5 должны быть затянуты таким образом, чтобы газоотборное устройство усилием руки нельзя было переместить в уплотнительном устройстве.
1 – труба (Ø6х1), 2 – пластина, 3 – труба (Ø22х2), 4 – центрирующая накладка, 5 – труба (Ø32х2), 6 – штуцер.
Рисунок 2. Водоохлаждаемое газоотборное устройство
Склянку 21 поднимают выше аспиратора. Открывают нижний, а затем верхний кран пипетки и заполняют ее запирающей жидкостью до верхнего крана, вытесняя воздух из пипетки в атмосферу через находящийся в положении «а» трехходовой кран и резиновую трубку 20.
Осуществляют промывку газоотборной линии отбираемым для анализа газом. Для этого склянку 21 опускают ниже аспиратора 19 и одновременно устанавливают трехходовой кран в положение «б». Запирающая жидкость перетекает из пипетки в склянку 21, а пипетка заполняется газом. Когда жидкость в пипетке приблизится к нижнему крану пипетки, склянку 21 поднимают выше аспиратора, одновременно переводя трехходовой кран в положение «а». При этом запирающая жидкость вытесняет набранный в пипетку газ в атмосферу. Промывку – отбор анализируемого газа в пипетку и вытеснение его в атмосферу – повторяют несколько раз.
Необходимое количество операций промывки определяют по формуле
M ≥ 4Vл/Vг,
где Vл – объем газоотборной линии (газоотборной трубки, патрона, резиновых трубок); Vг – объем пипетки.
Когда последний «промывочный» объем газа вытеснен из пипетки в атмосферу, отбирают пробу газа для анализа. Для этого склянку 21 опускают ниже аспиратора 19, одновременно переводя трехходовой кран в положение «б». После заполнения пипетки газом (при этом запирающая жидкость не должна опускаться до нижнего крана) закрывают ее верхний кран, склянку 21 поднимают выше аспиратора и таким образом создают в пипетке избыточное давление. Закрывают нижний кран пипетки и устанавливают трехходовой кран в положение «а», после чего резиновую трубку 18 снимают с пипетки.
После отбора проб склянку 21 устанавливают в гнездо аспиратора, аспиратор закрывают крышками и транспортируют в помещение, предназначенное для анализа. Пробы газ хранят в аспираторе при комнатной температуре. Во время хранения склянку 21 ставят выше аспиратора, а нижние краны пипеток открывают.
2. Нахождение поправочного коэффициента начнем с анализа водоохлаждающего пробоотборника.
Примем, что начальная температура охлаждающего теплоносителя не изменяется, то есть Т1=const. Температура смеси в газоотборной линии Т в начале процесс равна Т0 , в конце периода охлаждения равна ТА.
Количество тепла, отнимаемое водой определяется по формуле:
где W1
– тепловая емкость воды,
![]() -
здесь К – среднее значение коэффициента теплопередачи, F
– поверхность теплообмена, τ – время охлаждения.
-
здесь К – среднее значение коэффициента теплопередачи, F
– поверхность теплообмена, τ – время охлаждения.
С другой стороны, потеря тепла вызывает падение температуры смеси в газоотборнике согласно уравнению, не учитывающему тепловую емкость стенок:
где W2 – тепловая емкость смеси.
Приравнивая правые части уравнения (1) и (2), и проинтегрировав их по времени и по температуре получим:
Из уравнения (3) находится время охлаждения τ смеси.
Будем считать, что газовая смесь в точке отбора пробы находится в состоянии химического равновесия. Тогда ее состав может быть определен при решении уравнений химического равновесия рассмотренных в работе [1]. Давление и температуру при этом считаем известными, также считаем известной температуру на входе в анализатор. Для простоты будем считать, что закон охлаждения пробы в канале зонда является известной функцией времени:
где
![]() ,
,![]() –
соответственно температура в точке отбора пробы и на входе в
анализатор;
–
соответственно температура в точке отбора пробы и на входе в
анализатор;
τ х–
время охлаждения с учетом химических реакций;
![]() ,
,
![]() -
скорость охлаждения в К/с;
-
скорость охлаждения в К/с;
Для нейтрализации концентрации оксида углерода СО в высокотемпературную газовую смесь впрыскивается водяной пар. Неравновесное протекание химических реакций между компонентами смеси описывается уравнениями химической кинетики.
где
![]()
![]() - массовая концентрация i – компоненты, р – давление, Т-
температура, n-
количество компонент, правая часть этого уравнения определена в
работе [2]. Здесь
- массовая концентрация i – компоненты, р – давление, Т-
температура, n-
количество компонент, правая часть этого уравнения определена в
работе [2]. Здесь
![]() (р,Т,
(р,Т,![]() )
=
)
=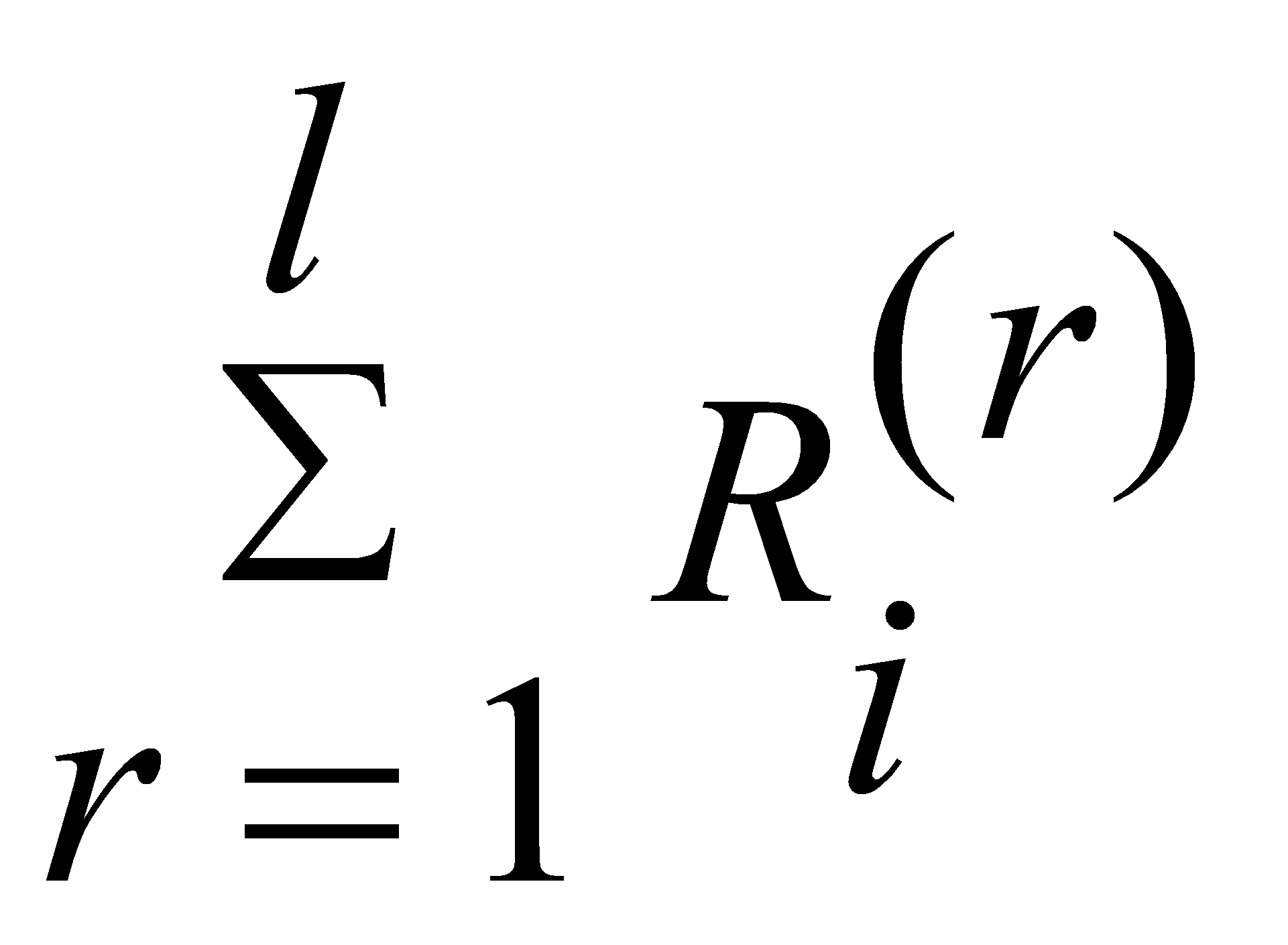 - массовая скорость образования вещества в
результате всех
- массовая скорость образования вещества в
результате всех
![]() реакций, с молекулярным весом
реакций, с молекулярным весом
![]() в ходе r
– реакций.
в ходе r
– реакций.
Для уравнения химической кинетики использована конечно-разностная схема предложенная в работе [2 ].
где &#; - параметр неявности схемы (обычно &#;</FONT> = 0,4), <SPAN LANG="en-US">h</SPAN><SUB><SPAN LANG="en-US">n</SPAN></SUB> – шаг интегрирования.<P> Таким образом, численное интегрирование системы уравнений химической кинетики (5<I>)</I> при заданной временной зависимости температур (4) дает нам зависимость концентрации оксида углерода от скорости охлаждения (рисунок 3). Далее находится поправочный коэффициент. <P><SPAN LANG="en-US">F</SPAN><SUB><SPAN LANG="en-US">x</SPAN></SUB>=<SPAN LANG="en-US">τ</SPAN><SUB><SPAN LANG="en-US">x</SPAN></SUB><SUB> </SUB>/ <SPAN LANG="en-US">τ</SPAN> (7)<P> где <SPAN LANG="en-US">τ</SPAN><SUB><SPAN LANG="en-US">x</SPAN></SUB> – время охлаждения, которое определяется из уравнения (4). <P><A HREF="images/m6258223d.gif" TARGET="_blank"><IMG src="https://articles-static-cdn.moluch.orgimages/m6258223d.gif" NAME="Объект21" ALIGN=BOTTOM WIDTH=294 HEIGHT=252></A><P> Рисунок 3. Зависимость весовой доли концентрации <SPAN LANG="en-US">CO</SPAN> от температуры<P> продуктов сгорания<P> <BR /> <DL> <DT><P>3. Концентрация оксида углерода (С<SUB>х</SUB> % по объему) в рабочей дозе рассчитывается по формуле:<DT><P> С<SUB>х</SUB> = <A HREF="images/58a55ed1.gif" TARGET="_blank"><IMG src="https://articles-static-cdn.moluch.orgimages/58a55ed1.gif" NAME="Объект22" ALIGN=ABSMIDDLE WIDTH=97 HEIGHT=45></A>, (8)</DL> <P> где <SPAN LANG="en-US">V</SPAN><SUB>СО</SUB> – объем введенного калибровочным микродозатором чистого оксида углерода, см<SUP>3</SUP>; <SPAN LANG="en-US">V</SPAN><SUB>Р.Д.</SUB> – объем рабочей дозы, см<SUP>3</SUP>, <SPAN LANG="en-US">F</SPAN><SUB><SPAN LANG="en-US">x</SPAN></SUB> поправочный коэффициент.<P> После проведения анализа исследуемого газа, содержащего оксид углерода в неизвестном количестве С<SUB>х</SUB>, замеряется высота пика на хроматограмме с учетом масштаба шкалы и по калибровочной зависимости определяется количество оксида углерода в анализируемом газе.<P> При использовании калибровочного газа с содержанием оксида углерода меньше 100% результат анализа, полученный при использовании калибровочной зависимости, должен быть умножен на коэффициент К = С<SUB>а</SUB>/100, где С<SUB>а</SUB> – концентрация оксида углерода в калибровочном газе, %.<P> Результат измерения должен быть представлен в следующем виде: <A HREF="images/m40200f9e.gif" TARGET="_blank"><IMG src="https://articles-static-cdn.moluch.orgimages/m40200f9e.gif" NAME="Объект23" ALIGN=ABSMIDDLE WIDTH=27 HEIGHT=21></A>±δ. Здесь <A HREF="images/m40200f9e.gif" TARGET="_blank"><IMG src="https://articles-static-cdn.moluch.orgimages/m40200f9e.gif" NAME="Объект24" ALIGN=ABSMIDDLE WIDTH=27 HEIGHT=21></A> – среднее арифметическое значение из <SPAN LANG="en-US">n</SPAN>-определений; δ – абсолютная погрешность измерения, характеризующая точность результата<P> δ = <A HREF="images/m1e1748a3.gif" TARGET="_blank"><IMG src="https://articles-static-cdn.moluch.orgimages/m1e1748a3.gif" NAME="Объект25" ALIGN=ABSMIDDLE WIDTH=31 HEIGHT=39></A>, (9)<P> где <SPAN LANG="en-US">t</SPAN> – табличное значение коэффициента Стьюдента при доверительной вероятности р=0,95; <SPAN LANG="en-US">n</SPAN> – число определений; <SPAN LANG="en-US">S</SPAN> – среднее квадратичное отклонение по всему массиву <SPAN LANG="en-US">n</SPAN>-определений;<P> <A HREF="images/28f9007c.gif" TARGET="_blank"><IMG src="https://articles-static-cdn.moluch.orgimages/28f9007c.gif" NAME="Объект26" ALIGN=ABSMIDDLE WIDTH=131 HEIGHT=48></A>, (10)<P> здесь Х<SUB><SPAN LANG="en-US">i</SPAN></SUB> – единичное определение.<P> Результаты, отличающиеся друг от друга более чем на ±δ, считают грубой ошибкой и исключают из рассмотрения. Значение δ надо рассчитывать для каждой серии параллельных определений. Относительная погрешность измерения ±5%.<P> Процентное содержание оксида углерода пересчитывают в мг/м<SUP>3</SUP> (при нормальных условиях) по формуле:<P> С<SUB>СО</SUB> = <A HREF="images/m40200f9e.gif" TARGET="_blank"><IMG src="https://articles-static-cdn.moluch.orgimages/m40200f9e.gif" NAME="Объект27" ALIGN=ABSMIDDLE WIDTH=27 HEIGHT=21></A><SUP>.</SUP>1,165<SUP>.</SUP>10<SUP>4</SUP>, (11)<P> где 1,165 – плотность оксида углерода (кг/м<SUP>3</SUP>) при нормальных условиях.<P> <BR /> <B>Литература:</B> <OL> <LI><P>Волков В.А. Расчет равновесного состава смеси реагирующих газов при заданном внешнем давлении. В кн. «Математические аспекты задач охраны воздушного бассейна». М.: Изд-во МАИ, 1984, с. 3-11.<LI><P> Пирумов У.Г. Обратная задача теории сопла. М:Машиностроение, 1988, 238с.<LI><P> Пирумов У.Г., Папуша А.И., Мусин В.Р. и др. Некоторые математические проблемы охраны воздушного бассейна. «Изв. АН СССР. Механика жидкости и газа». 1981, 202 с.</OL>